ถ้าอะตอมคู่ร่วมพันธะใช้อิเล็กตรอนร่วมกัน 2 คู่จะเกิดเป็นพันธะโคเวเลนต์ที่เรียกว่า พันธะคู่ เช่น ในโมเลกุลของออกซิเจนถ้าอะตอมคู่ร่วมพันธะใช้อิเล็กตรอนร่วมกัน 3 คู่จะเกิดเป็นพันธะโคเวเลนต์ที่เรียกว่า พันธะสาม เช่น ในโมเลกุลของไฮโดรเจน
จากการศึกษาสารโคเวเลนซ์จะพบว่า ธาตุที่จะสร้างพันธะโคเวเลนต์ส่วนมากเป็นธาตุอโลหะกับอโลหะ ทั้งนี้เนื่องจากโลหะมีพลังงานไอออไนเซชันค่อนข้างสูง จึงเสียอิเล็กตรอนได้ยาก เมื่ออโลหะรวมกันเป็นโมเลกุลจึงไม่มีอะตอมใดเสียอิเล็กตรอน มีแต่ใช้อิเล็กตรอนร่วมกันเกิดเป็นพันธะโคเวเลนต์ อย่างไรก็ตามโลหะบางชนิดก็สามารถเกิดพันธะโคเวเลนต์กับอโลหะได้ เช่น Be เกิดเป็นสารโคเวเลนซ์คือ BeCl2เป็นต้นชนิดของพันธะโคเวเลนต์
อะตอมที่เกิดพันธะ นักเคมีนิยมใช้การเขียนสัญลักษณ์แบบจุดของลิวอิส โดยประกอบด้วยสัญลักษณ์แทนนิวเคลียสกับอิเล็กตรอนในชั้นถัดจากเวเลนซ์อิเล็กตรอนเข้าไป และจุดรอบสัญลักษณ์แทนจำนวนเวเลนซ์อิเล็กตรอนของธาตุนั้น ๆ
ชนิดของพันธะโคเวเลนต์
พิจารณาจากจำนวนอิเล็กตรอนที่ใช้ร่วมกันของอะตอมคู่ร่วมพันธะ ดังนี้
ก. พันธะเดี่ยว เป็นพันธะโคเวเลนต์ที่เกิดจากอะตอมคู่สร้างพันธะทั้งสองใช้อิเล็กตรอนร่วมกัน1 คู่ ใช้เส้น ( - ) แทนพันธะเดี่ยว
ข. พันธะคู่เป็นพันธะโคเวเลนต์ที่เกิดจากอะตอมคู่สร้างพันธะทั้งสองใช้อิเล็กตรอนร่วมกัน 2 คู่ ใช้เส้น 2 เส้น (= ) แทน 1 พันธะคู่ เช่น พันธะระหว่าง O ใน O2, O กับ C ใน CO2, C กับ H ใน C2H4
ค. พันธะสามเป็นพันธะโคเวเลนต์ที่เกิดจากอะตอมคู่สร้างพันธะทั้งสองใช้อิเล็กตรอนร่วมกัน 3 คู่ ใช้เส้น 3 เส้น ( = ) แทน 1 พันธะสาม เช่น พันธะระหว่าง N กับ N ใน N2 , N กับ C ใน HCN
ชนิดของพันธะโคเวเลนต์
อะตอมที่เกิดพันธะ นักเคมีนิยมใช้การเขียนสัญลักษณ์แบบจุดของลิวอิส โดยประกอบด้วยสัญลักษณ์แทนนิวเคลียสกับอิเล็กตรอนในชั้นถัดจากเวเลนซ์อิเล็กตรอนเข้าไป และจุดรอบสัญลักษณ์แทนจำนวนเวเลนซ์อิเล็กตรอนของธาตุนั้น ๆ
ชนิดของพันธะโคเวเลนต์ พิจารณาจากจำนวนอิเล็กตรอนที่ใช้ร่วมกันของอะตอมคู่ร่วมพันธะ ดังนี้
ก. พันธะเดี่ยว เป็นพันธะโคเวเลนต์ที่เกิดจากอะตอมคู่สร้างพันธะทั้งสองใช้อิเล็กตรอนร่วมกัน
1 คู่ ใช้เส้น ( - ) แทนพันธะเดี่ยว เช่น

ข. พันธะคู่เป็นพันธะโคเวเลนต์ที่เกิดจากอะตอมคู่สร้างพันธะทั้งสองใช้อิเล็กตรอนร่วมกัน 2 คู่ ใช้เส้น 2 เส้น (= ) แทน 1 พันธะคู่ เช่น พันธะระหว่าง O ใน O2, O กับ C ใน CO2, C กับ H ใน C2H4

ค. พันธะสามเป็นพันธะโคเวเลนต์ที่เกิดจากอะตอมคู่สร้างพันธะทั้งสองใช้อิเล็กตรอนร่วมกัน 3 คู่ ใช้เส้น 3 เส้น ( = ) แทน 1 พันธะสาม เช่น พันธะระหว่าง N กับ N ใน N2, N กับ C ใน HCNตาราง โครงสร้างลิวอิสของโมเลกุลโคเวเลนต์บางชนิด

พันธะโคออร์ดิเนตโคเวเลนต์ คือ พันธะโคเวเลนต์ที่เกิดจากการใช้อิเล็กตรอนร่วมกันของอะตอมโดยอิเล็กตรอนคู่นี้มาจากอะตอมใดอะตอมหนึ่งไม่ได้มาจากทั้ง 2 อะตอม การเกิดพันธะจะเกิดเมื่อเกิดพันธะโคเวเลนต์ตามปกติ แล้วยังมีอะตอมใดอะตอมหนึ่งที่เวเลนซ์อิเล็กตรอนยังไม่ครบตามกฎออกเตต
โมเลกุลที่ไม่เป็นไปตามกฏออกเตด1. อิเล็กตรอนรอบอะตอมกลางน้อยกว่า 8 ในสารประกอบบางชนิด จำนวนอิเล็กตรอนที่ล้อมรอบอะตอมกลางมีจำนวนน้อยกว่าแปด เช่น เบอร์ริลเลียม ซึ่งเป็นธาตุหมู่ 2A ซึ่งมีการจัดเรียงอิเล็กตรอนเป็น 1s22s2 มีเวเลนซ์อิเล็กตรอน 2 ตัว อยู่ที่ออร์บิตัล 2s ในสภานะแก๊ส เบอร์ริลเลียมไฮไดรด์ (BeH2)เป็นโมเลกุลที่เสถียรโดยมีโครงสร้างลิวอิสดังรูป
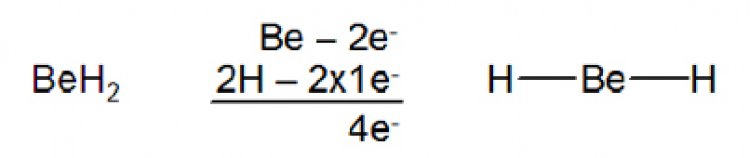
เห็นได้ว่า ที่อะตอมกลางมีเพียง 4 อิเล็กตรอนเท่านั้น ส่วนโบรอนซึ่งเป็นธาตุหมู่ 3A ที่อะตอมกลางของ BF3ก็มีเพียง 6อิเล็กตรอนเท่านั้น
2 โมเลกุล บางชนิดมีจำนวนอิเล็กตรอนเป็นเลขคี่ เช่น nitric oxide (NO) และ nitrogen dioxide (NO2)
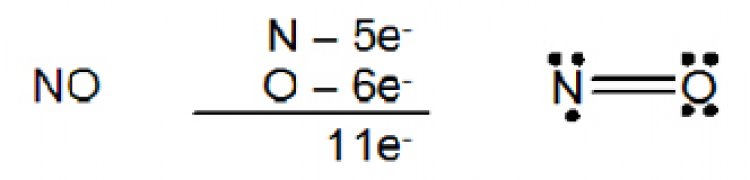
3. อิเล็กตรอนรอบอะตอมกลางมากกกว่า 8เกิดในกรณีที่อะตอมกลางเป็นธาตุในคาบที่สามเป็นต้นไป ซึ่งธาตุเหล่านี้มี 3d ออร์บิตัลที่ว่าง สามารถรับอิเล็กตรอนเพื่อสร้างพันธะได้ด้วย ตัวอย่างเช่น SF6 ซึ่งอะตอมกลางมีอิเล็กตรอน 12 ตัว ล้อมรอบ

ที่มา : คลิกที่นี
หน้าต่อไป : คลิกที่นี่


ไม่มีความคิดเห็น:
แสดงความคิดเห็น